Entzimen zinetika
Entzimen zinetikak entzimek katalizatzen dituzten erreakzio biokimikoen abiadura aztertzen du. Jakina denez, entzimek erreakzio horien abiadura areagotzen dute substratuen aktibazio energia jaisten dutelako.
Aktibazio energia erreakzionatuko duten molekulei beren lotura kimikoak apurtzeko eman behar zaien energiari deritzo. Lotura kimikoen arabera aldatzen du aipatutako aktibazio energiak: lotura ioniko batean energia hori oso txikia da (ClNa, esaterako, erraz disoziatzen da Na+ eta Cl--an). Lotura kobalente bat apurtzeko, aldiz, aktibazio-energia askoz handiagoa da.
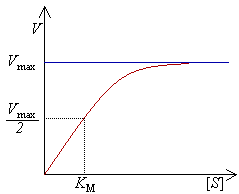
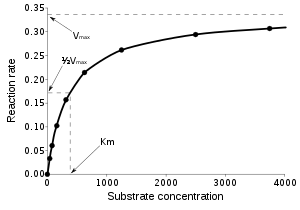
Entzimen zinetikak eskuineko irudian agertzen den mota horretako grafikoa osatzen du. Ikusten denez, entzimaren kontzentrazioa konstantea bada, substratuaren kontzentrazioa handitu ahala erreakzio biokimikoaren abiadura areagotzen da, harik eta substratu-kontzentrazio jakin bateraino iritsi arte. Gero abiadura gelditzen da entzimaren asetasuna gertatzen delako: ez dago nahiko entzimarik gehiegizko substratu horrekin erreakzionatzeko, entzima/substratu konplexua (ES) sortzeko.
Substratuaren kontzentrazioa oso handia denean entzimak asetu ohi dira. Entzima guztien gune aktiboak substratuz beteta daudenez, ez dira ES konplexu gehiago sortuko, eta beraz ez da produktu gehiago agertuko. Substratu molekulek entzima molekula guztiak hartu dituztenean erreakzioaren abiadura maximoa lortzen da, eta abiadura hori ez da gaindituko ezta substratu molekula gehiago gehituta ere.
Michaelis-Mentenen ekuazioa[aldatu | aldatu iturburu kodea]
Asetasunaren ondorioak aztertzean, Michaelisek eta Mentenek entzima eta substratuaren arteko lotura ikertu zuten: substratuaren (S) kontzentrazioa handitzen denean entzima guztiek (E) entzima/substratu (ES) konplexura pasatuko dute. Konplexu honetatik agertuko da erreakzioaren produktua (P):

Entzimen zinetikaren lehenengo ekuazio orokorra, beraz, honako hau izaten da:
Entzima/substratu (ES) konplexuaren sortze-abiadura hau izanen da:
ES konplexuaren sortze eta desagertze prozesuak orekan daudenean honako hau beteko da:
Eta hortik abiatuta emaitza honetara iristen da:
Era berean, Michaelis-Mentenen konstantea horrela definitzen da:
Beraz:
(1)
Erreakzioaren abiadura hau da:
(2)
Eta entzimaren konzentrazio osoa:
Beraz:
(3)
(3) (1)-ean ordezkatuz:
Eta:
(4)
(4) (2)-an ordezkatuz :
Azken balore hau Michaelis-Menten deritzon ekuazioa da. Hortik abiatuta, erraz frogatzen da erreakzioaren abiadura abiadura maximoaren erdia bada:
Irudian ikusten denez, abiadura maximoaren erdia lortzeko behar den substratuaren kontzentrazioa da. Konstante hori handia izateak esan nahi du abiadura maximoaren erdia lortzeko substratuaren kontzentrazio handia behar dela eta, beraz, entzimak ez duela afinitate handirik substratu horrekiko


![{\displaystyle {\frac {d[ES]}{dt}}=k_{1}[E][S]-k_{-1}[ES]-k_{2}[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e90d1004d5c06ccd4198e2143b928b04ae09f59c)
![{\displaystyle {\frac {d[ES]}{dt}}=k_{1}[E][S]-k_{-1}[ES]-k_{2}[ES]=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2bb19158ff794158ceac860552fbfa1eacdf3558)
![{\displaystyle [ES]={\frac {k_{1}[E][S]}{k_{-1}+k_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/041c97c8ca3aa792f4fe79f75ec6b88ba19098aa)

![{\displaystyle [ES]={\frac {[E][S]}{K_{m}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6ae6e75fd92aa67bd80cf22f780cdb231efacee1)
![{\displaystyle {\frac {d[P]}{dt}}=k_{2}[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0fc45725f2f145f603fcf61641d533d1bbcdb70d)
![{\displaystyle [E_{0}]=[E]+[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/98b6b65c6ec79a6eb4bdb476e877e3acfb8c6503)
![{\displaystyle [E]=[E_{0}]-[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ba5fa93cfdb8b7ffec08ac9d5892a6df7b7c1694)
![{\displaystyle [ES]={\frac {([E_{0}]-[ES])[S]}{K_{m}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af25e5b446ab5bb7cf963aa5c695540414dd272a)
![{\displaystyle K_{m}[ES]+[S][ES]=[E_{0}][S]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/823baafd833a562d3cf260b519b7c8b3f01afef4)
![{\displaystyle [ES]={\frac {[E_{0}][S]}{K_{m}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b3ab5a4bda584bb8c9de0f0eaf00e89e8295f81d)
![{\displaystyle {\frac {d[P]}{dt}}=k_{2}[E_{0}]{\frac {[S]}{K_{m}+[S]}}=V_{max}{\frac {[S]}{K_{m}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/230401cdb47fc5cdca32646aacbc167e546a7d79)
![{\displaystyle {K_{m}=[S]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/be6831964a5c57e532d050822040a678cc10e6f8)