Hidrolisi: berrikuspenen arteko aldeak
t Robot: Cambios triviales |
t robota Erantsia: io:Hidrolizo |
||
| 24. lerroa: | 24. lerroa: | ||
[[fr:Hydrolyse]] |
[[fr:Hydrolyse]] |
||
[[he:הידרוליזה]] |
[[he:הידרוליזה]] |
||
[[io:Hidrolizo]] |
|||
[[it:Idrolisi]] |
[[it:Idrolisi]] |
||
[[ja:加水分解]] |
[[ja:加水分解]] |
||
07:24, 10 uztaila 2009ko berrikusketa
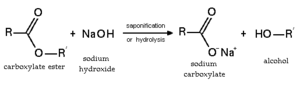
Hidrolisia, ura eta substantzia baten artean gertatzen den erreakzio kimikoa da. Erreakzio hau jasan dezaketen substantzien artean, gatzak daude, uretan disolbatzerakoan, gatz horiek osatzen dituzten ioiek, hidronio edo oxonio H3O+ ioiekin konbinatzen dira, edo hidroxilo OH- ioiekin, edo biekin. Ioi horiek, uraren disoziazio edo autoprotolisitik datoz. Honek, uraren disoziazioaren orekaren alderatze bat eragiten du, eta, ondorioz, pHaren balioa aldatzen da.
Azido edo base ahulen gatzak, uraren ondorioz hidrolizatzen dira, erreakzioaren maila, azido edo basearen ahultasunaren araberakoa delarik. Hau da, azidoa edo basea zenbat eta ahulagoa izan, hainbat eta handiagoa da hidrolisia.
H2O formula duen uraren molekula batek, AB substantzia batekin erreakzionatzen duen erreakzio kimiko mota bat ere bada, non Ak eta Bek, atomoak edo atomo taldeak irudikatzen dituzten. Erreakzioan, uraren molekula H+ eta OH- zatietan banatzen da, eta AB molekula, A+ eta B- zatietan. Jarraian, zati hauek, AOH eta HB amaierako produktuak emanez elkartzen dira. Erreakzio mota hau, sarri, deskonposaketa bikoitza edo elkartrukea deitzen da. Interes berezikoa da disolbaketa azido edo basikoak sortzen dituzten zenbait gatzen hidrolisia.
