Infragorrien espektroskopia
|
|
edo atal hau ez dator bat formatu hitzarmenekin. |

Infragorrien espektroskopia molekulen bibrazio mailekin lotuta dago. Maila hauen arteko eszitazioak eragiteko, infragorrizko argiaren energia beharrezkoa da. Argi mota hau erabiliz gauzatzen den espektroskopiari espektroskopia infragorria deritzo, ala bibrazio espektroskopia. Azkenekoak, parte hartzen duten maila molekular motei aipua egiten dio. Lehenengoak, aldiz, hauen artean trantsizioak eragiteko behar den argi motari. Espektroskopia infragorria (bibrazio espektroskopia edo IR espektroskopia) elkartzen du erradiazio infragorriaren interakzioa materiarekin. Honetarako teknika asko biltzen dira, batez ere xurgapen espektroskopian oinarrituta.
Teknika espektroskopiko guztiak bezala, substantzia kimikoak aztertzeko erabil daiteke. Muestrak solidoak, gasak edo likidoak izan daitezke. Espektroskopia infragorriaren metodoa espektrometro infragorria izeneko tresna batekin egiten da (espektrofotometroa). Horrela infragorria espektroa sortzen da. Infragorri espektroa, argi infragorriaren xurgapenaren grafiko batean ikusi ahal da. Grafikoan ardatz bertikalean argi infragorriaren xurgapena aipatuko da eta frekuentzia edo uhin-luzera ardatz horizontalean.
IR espektro baten frekuentzia unitateei dagokienez, uhin-zenbakiak erabiltzen dira( cm-1). Infragorriaren uhin-luzeraren unitateei dagokienez mikrometroak erabiltzen dira. Laborategian aztertzen den ohiko teknika bat Fourier Transform Infrared Spectrometer (FTIR) da.
Espektro elektromagnetikoaren infragorri zatiak, hiru eskualdeetan banatzen dira, hurbileko infragorriaren eskualdea, erdiko eskualdea eta urrutiko eskualdea. Eskualdeak, ikusle espektroarekin daukaten harremanaren araberaz izendatutak daude. Hurbileko infragorriaren eskualdearen energiarik handiena 14000-4000 cm-1 bitartekoa da gutxi gorabehera (0.8-2.5 µm uhin-luzera). Energia honek, bibrazio harmonikoak kitzikatzen ditu. Erdiko eskualdearen energia 4000-400 cm-1 bitartekoa da (2.5-25 µm) eta oinarrizko bibrazioak eta haien errotazio-bibrazio egitura aztertzeko erabiltzen da. Azkenik, urruneko eskualdearen energia 400-100 cm-1 bitartekoa da (25-1000 µm). Mikro-uhinen eskualdetatik hurbil dago eta gutxieneko energia duena, errotazio-espektroskopia aztertzeko erabiltzen da.
Teoria[aldatu | aldatu iturburu kodea]
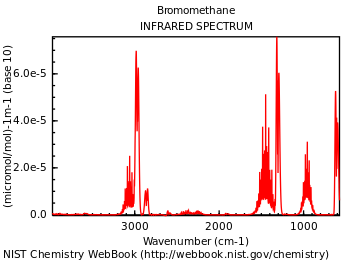
Molekulek beraien egitura kimikoaren arabera frekuentzia ezberdinetan absorbatzen dute, eta fenomeno honetan, hain zuzen ere, oinarritzen da espektroskopia infragorria. Absortzio hauek frekuentzia erresonanteetan gertatzen dira, hau da, absorbatutako erradiazioaren frekuentzia eta frekuentzia bibrazionala bat datoz. Energiak, atomoen masen, akoplamendu bibrazionalen eta energia potenzial molekularrak daukan azaleraren eragina daukate.
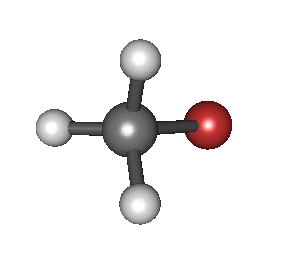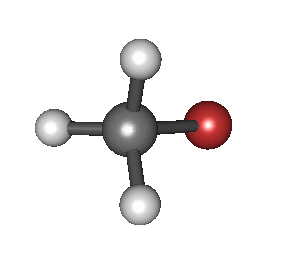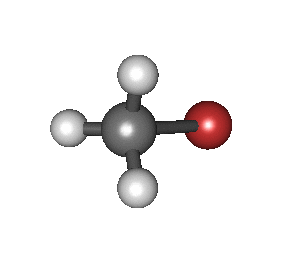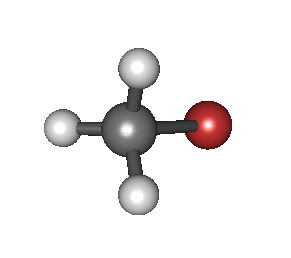
Bereiziki, Born-Oppenheimer hurbilketan eta hurbilketa harmonikoetan, hau da, Hamiltondar molekularra egoera fundamental elektronikoari dagokionean, hurbilketa egin ahal da osziladore harmoniko batekin. Frekuentzia erresonanteak, egoera fundamental elektroniko molkularraren energia potentzialaren modu normalekin zerikuzia dute. Frekuentzia erresonanteak, loturaren indarrarekin eta atomoen masarekin erlazionatuta daude.
Modu bibrazionalen zenbakiak[aldatu | aldatu iturburu kodea]
Lagin bateko bibrazio-modu bat IR-en aktiboa izateko, momentu dipolarreko aldaketekin loturik egon behar da. Ez da beharrezkoa dipolo iraunkor bat, arauak momentu dipolarrean aldaketa bat soilik eskatzen baitu.
Molekula batek era askotan bibratu dezake, eta modu horietako bakoitzari modu bibrazional deritzogu. N atomo dituzten molekulentzat; molekula linealek 3N-5 modu bibrazionalen gradu dituzte, molekula ez linealek, aldiz, 3N-6. Adibidez, ura (H2O), molekula ez lineala izanik, 3x3-6 = 3 modu bibrazionalen gradu izango lituzke.
Molekula diatomiko simpleek lotura eta banda bibrazional bakarra dituzte. Molekula simetrikoa bada, adibidez N2-ren kasuan, honen absortzio banda ezin izango da IR espektro batean antzeman, hau ikusteko aukera bakarra Raman espektro baten bitartez izango da. Molekula diatomiko asimetrikoek, CO-k adibidez, IR espektroan absorbatzen dute. Molekula konplexuagoek lotura ugari dituzte, hortaz, hauei dagokien espektro bibrazionalek konplexutasun maila handiagokoak dira, hau da, molekula handien IR espektroetan piko ugari antzematen dira.
Normalean konposatu organikoetan aurkitu daitekeen CH2X2 taldeko atomoak, non X beste edozer atomo izan daitekeen, bederatzi modu ezberdinetan bibratu dezakete. Bibrazio modu hauetako sei CH2 taldeari soilik dagokiete: luzapen simetriko eta antisimetrikoa (symmetric and antisymmetric stretching), artazia (scissoring), kulunka (rocking), eragina (wagging) eta bira (twisting). X talde gehigarriak ez dituzten egiturek modu bibrazional gutxiago dituzte, modu hauetako batzuk talde horiekiko erlazio espezifikoetan oinarrituta daudelako. Adibidez, uretan, rocking, wagging eta twisting moduak ez dira existitzen, H atomoen mogimendu motek molekularen errotazio sinplea errepresentatzen baidute, eta ez honen barneko bibrazioak.
| Symetry
/ Direction |
Symmetric | Antisymmetric |
|---|---|---|
| Radial | 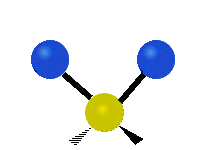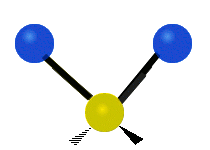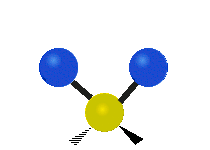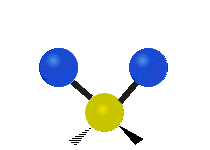 Symmetric stretching |
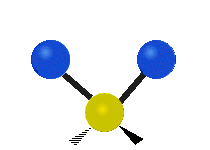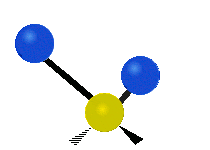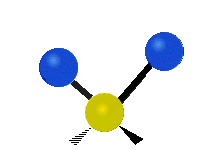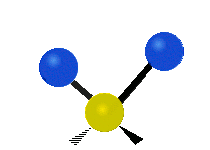 Antisymmetric stretching |
| Latitudal |  Scissoring |
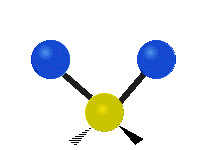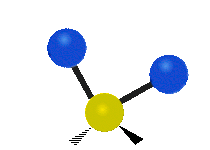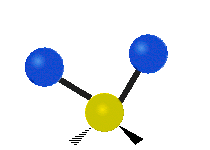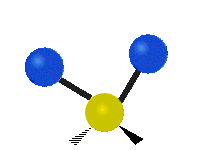 Rocking |
| Longitudal |  Wagging |
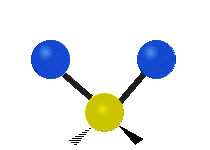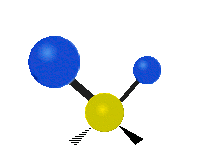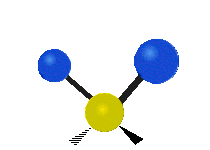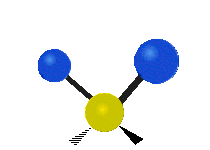 Twisting |
Efektu espezialak[aldatu | aldatu iturburu kodea]
IR banda sinple eta inportante edo fundamentalenak modu normalen exitaziotik datozte (molekularen distortzio sinpleenak), egoera fundamentaletik, zenbaki kuantiko bibratorio v=0 tik, leen egoera exitatura, non zenbaki kuantiko bibratorioa v=1 den. Kasu batzuetan, banda armonikoak antzeman daitezke. Banda armoniko bat fotoi baten absortzioaren ondorioz sortzen da, non trantsizio direkto baten bitartez egoera fundamentaletik bigarren egoera bibratorio exitatura (v=2) pasatzen den. Aipatutako banda armonikoa banda fundamentalaren energia bikoitzera, gutxi gorabehera, azaltzen da modu normal berdinerako. Exitazio batzuk, konbinazio modu deiturikoak, modu normal bat baino gehiagoren aldi bereko exitazioan oinarritzen dira. Fermiren erresonantzia fenomenoa, bi moduk energia antzerakoa dutenean sor daiteke; fermiren erresonantziak, banden energia eta intentsitatean ustekabeko aldaketak sortzen ditu.
Infragorri espektroskopia praktikoa[aldatu | aldatu iturburu kodea]
Lagin baten infragorri espektroa grabatzeko, infragorri argiaren izpia laginean zehar igaro behar du. IR frekuentzia lotura bikoitz baten edo zenbait loturen talde baten bibrazio frekuentziaren berdina denean, absortzioa gertatzen da. Transmititu den argia azterzean, frekuentzia edo uhin-luzera bakoitza xurgatu duen energia adierazten du. Neurketa honek monokromadore batekin gorde daiteke,hau da, uhin-luzeraren heina eskaneatzen. Uhin-luzeraren heina neurtzeko beste modu bat Fourier transformazio izeneko tresna da, honekin uhin-luzeraren hein osoa neurtzen da eta ondoren transmitantzia edo absorbantzia espektroa eratzen da.
Teknika hau ohikoa da lotura kobalentea duten laginak aztertzean. Espektro sinpleak purutasun handiko maila duten laginekin lortzen da. Baita infragorri lotura aktiboak dituztenak ere. Zenbat eta konplexuagoa izan egitura molekularra, orduan eta konplexuagoa izango da espektroa (absortzio-banda gehiago izango du.

Laginen prestakuntza[aldatu | aldatu iturburu kodea]
Gas Laginak ibilbide luzeko lagin zeldak behar dituzte beraien diluzioa konpensatzeko. Lagin zelden ibilbide luzera aztergai dugun konposatuaren kontzentrazioaren araberakoa izango da. Bi alboetan leiho infragorri transparenteak dituen 5-10 cm bitarteko luzeeradun kristalezko hodi sinple bat erabili daiteke zenbait ehunka ppm-ko kontzentrazioa duten laginen kasuan.
Lagin likidoak purutasun handiko gatz bat daukaten bi plaken artean prestatu daitezke. Normalean erabilitako gatza kloruro sodikoa da, baina bromuro potasikoa edo fluoruro kaltzikoa ere erabil dezakegu. Plakak infragorri argian gardenak dira, orduan ez dira espektroan agertuko. Zenbait plakak oso disolbagarriak dira uretan, horrela laginak anhidroak egon behar dira (urik gabe).
Lagin solidoak bi modutan prestatu daitezke. Lehenengoa lagina ehotzea eragile aglomeratzile batekin suspentsio bat sortzeko. Ondoren suspentsio honen zati bat gatz plaka batean aplikatzen da eta neurtzen da.
Bigarren modua, laginaren kantitate bat txikitzea da purua den gatz batekin (bromuro potasikoa). Hauts-nahaste hau trokel prentsa mekaniko batean txikitzen da pilula zeharrargi bat sortzeko. Honen bidez, espektrometroaren argi izpia pasatzen da.
Laginen prestakuntzan lortutako espektroak desberdinak izango dira haien artean laginen egoera fisikoengatik, hala ere, zenbait kasutan, eragile aglomeratzaileek infragorrian absorbatzen dute, banda nabarmen batzuk emanez.
Erreferentzia batekin konparatzea[aldatu | aldatu iturburu kodea]

Ohikoa da laginaren eta "erreferantziaren" espektroa lortzea. Atal hau zenbait aldagarri zuzentzeko gauzatzen da, adibidez, infragorri detektagailua (espektroan eragina izango du). Erreferentziaren neurketa tresnaren influentzia deuseztazea baimenduko du.
Erreferentzia egokia, neurketaren eta honen hekburuaren menpe dago. Erreferentziarik sinpleena bakarrik lagina bazterzteko erabiltzen da. Hala ere, batzuetan erreferentzia desberdinak baliagarriagoak dira. Adibidez, lagina matraze batean uretan disolbatuta dagoen solutu bat bada, erreferentziaren neurketa egokia matrazean dagoen ur purua neurtzea baimenduko du. Ondoren, erreferentziaren neurketak tresnaren ezaugarriak ezabatuko ditu. Neurketa honek matrazearen argi-absortzio eta argi-islapen ezaugarriak ere ezabatuko ditu. Ondorioz jakingo dugu solutuaren ezaugarriak.
Erreferentzia konparatzeko, modu sekuentziala gauzatzen da. Lehenengo pausoa erreferentzia neurtzea da, ondoren erreferentzia laginarekin aldatzen da eta lagina neurtzen da. Teknika hau ez da guztiz fidagarria. Horretarako beste metodo batzuk erabiltzen dira, adibidez, sorta-bikoitz metodoa. Metodo honek zehaztazuna hobetzen du eta akatzak txikitzen ditu. Beste aldetik, akats hauek estadistikoki hobetzeko estandar-adikzioa burutzen da.
FTIR[aldatu | aldatu iturburu kodea]
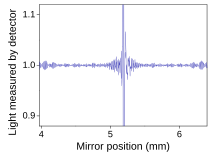
Espektroskopia infragorriaren Fourier transformazioa (FTIR), Infragorri espektro bat lortzeko erabiltzen den neurketa-teknika da. Argi infragorria interferometro batetik zehar igaro eta ondoren laginean barrena joaten da ( edo alderantziz). Tresnaren barruan ispilu mugikor bat dago, eta honen bitartez, interferometrotik pasatzen den infragorri argiaren kokapena aldatzen da. Orduan seinalea lortzen dugu, “interferograma” izenekoa. Interferograma, argiaren kanporaketa ispiluaren posizioaren menpe adierazten du. Fourier transformazio izeneko datu-prozesamendu teknikak prozesatu ez diren datuak nahi dugun datuetan bihurtzen ditu ( laginaren espektroa): argiaren kanporaketa, infragorri uhin-luzeraren menpe adierazten da. Laginaren espektroa beti erreferentziarekn konparatzen da.
Espektroskopia infragorriaren Fourier transformazioa (FTIR), Infragorri espektro bat lortzeko erabiltzen den neurketa-teknika da. Argi infragorria interferometro batetik zehar igaro eta ondoren laginean barrena joaten da ( edo alderantziz). Tresnaren barruan ispilu mugikor bat dago, eta honen bitartez, interferometrotik pasatzen den infragorri argiaren kokapena aldatzen da. Orduan seinalea lortzen dugu, “interferograma” izenekoa. Interferograma, argiaren kanporaketa ispiluaren posizioaren menpe adierazten du. Fourier transformazio izeneko datu-prozesamendu teknikak prozesatu ez diren datuak nahi dugun datuetan bihurtzen ditu ( laginaren espektroa): argiaren kanporaketa, infragorri uhin-luzeraren menpe adierazten da. Laginaren espektroa beti erreferentziarekn konparatzen da.
Espektroa lortzeko ordezko modu bat “monokromadore dispertsiboa” izeneko teknika da. Metodo honen bidez, lagina modu sekuentzialean irradiatzen da banakako uhin-luzera batzuekin. Metodo hau ohikoa da UV-Vis espektroskopian infragorrian baino, infragorri espektroskpian aldiz, askoz praktikoagoa da FTIR sistema.
Absortzio bandak[aldatu | aldatu iturburu kodea]
Espektroskopia infragorria molekulen egitura kimikoa identifikatzeko ere erabiltzen da. Espektro baten absortzio banden intentsitate eta posizioaren arabera (frekuentzia), molekulen talde funtzionalak anteman daitezke, hauetako bakoitzak banda karakteristikoak baititu. Banda hauen posizioa tauletako datuekin konparatuz jakin dezakegu zein talde funtzionalei dagokien.
Jatorrizko artikulua: Infrared spectroscopy correlation table (https://en.wikipedia.org/wiki/Infrared_spectroscopy_correlation_table)

Taulako uhin luzeerak cm−1-etan adierazita daude.
Badgerren erregela[aldatu | aldatu iturburu kodea]
Mota askotako laginen kasuan, hauen espektroetan aurkitzen diren banden asignazioak ezagunak dira, adb. zer maiztasunarekin asoziaturik dagoen zein lotura deformazio. Kasu horietan aztergai dugun lotura kimikoaren indarrari buruzko informazio gehiago lor dezakegu Badgerren arau deritzon gida empirikoari erreparatuz.
Richard Badgerrek 1934. urtean argitaratutako arau honek dio lotura kimiko baten indarra eralzionatuta dagoela bere modu bibrazioaren frekuentziarekin. Horrela, loturaren indarrak gora egin ahala, honi dagokion frekuentziak ere gora egingo du eta alderantziz.
Erabilera eta aplikazioak[aldatu | aldatu iturburu kodea]
Espektroskopia infragorria kimika organiko naiz inorganikoaren arloetan oso zabaldua dagoen teknika sinple eta fidagarria da, industria eta ikerkuntza munduan oso erabilia dena. Kalitate kontrolak eta neurketa medioanbientalak egiteko ohiko baliabidea da, adibidez, berotegi efektua kausatzen duen atmosferako CO2-aren kontzentrazioaren epe luzeko bilakaera aztertzeko.
Auzitegi analisietan ere erabiltzen da infragorrien espektroskopia, kasu zibil naiz kriminologikoetan, adibidez; polimero jakin baten degradazioa aztertzeko, edo auto gidari baten odoleko alkohol kontzentrazioa determinatzeko erabili daiteke.
Pintura eta koloredun eskuizkribuetako pigmentuen analisi eta identifikaziorako ere teknika baliagarria da.
Espektroskopia infragorria ikergai dugun lagin batean zer substantzia daukagun jakiteko erabili daiteke. Horretarako, aurrez egindako substantzia ezberdinen espektroen data-base batekin konparatuko dugu lortutako espektroa.
Espektroskopia infragorria polimeroen industrian ere garrantzi handikoa da. Bertan, polimeroen polimerizazio maila neurtzeko erabiltzen ohi da. Bestalde, polimero bateko lotura partikular baten izaera edo kantitatean gerta daitezkeen aldaketak aztertzeko ere erabiltzen da, denboran zehar polimeroaren frekuentzia ezberdineko IR epektroak eginez.
Gaur egungo ikerkuntza tresna modernoek ikergai duten frekuentzia multzoko IR espektroak oso modu bizkorrean neurtu ditzazkete, segunduko 32 neurketa eginez.
Elikagaien industrian ere erabiltzen da espektroskopia infragorria; elikagai ezberdinetan zenbait konposatu kimikoen kontzentrazioa neurtzeko.
Espektro infragorriak neurtzeko tresnak geroz eta tamaina txikiagokoak direnez, geroz eta errazagoa da huaen transporte eta erabilpena kale probetan.
Espektroskopia infragorria gasen isurketa detektatzeko gailuetan (DP-IR eta EyeCGAs) erabiltzen da. Instrumentu hauek, adibidez, hidrokarburoen gas isurketak detektatu ditzakete gas natural eta petrolioaren garraioetan.
204ko otsailean, NASAk hidrokarburo aromatiko poliziklikoen (PAH) IR espektroskopian oinarritutako datu base bat iragarri zuen, unibertsoaren jarraipena egiteko. Zientzialarien arabera, unibertsoaren karbonoaren %20 baino gehiago egon daiteke PAH konposatuetan, eta hauek bizimodua sortzeko hasierako material posibleak direla uste dute. PAHek badirudi Big Bang-aren ondoren sortu eta unibertso osoan hedatu zirela. Bestalde, izar berriekin eta exoplanetekin lotzen dira.
Azken berrikuntzek hodeian oinarritutako datu-base bati lotutako miniaturazko IR-espektrometro bat dakarte, eguneroko erabilera pertsonalerako pentsatua dagoena. Bestalde, NIR txip espektroskopikoak ere garatzen ari dira mugikor inteligenteetan itxatxi daitezkeenak, eta baita ere zenbait mugikor aplikazio.
Efektu isotopikoak[aldatu | aldatu iturburu kodea]
- Espezie partikular batek dauzkan isotopo desberdinak zehaztasun garrantzitsuak erakutsi ahal dituzte infragorri espektro batean. Adibidez, oxihemozianinaren O-O loturaren frekuentzia 832 eta 788 cm-1 baloreak hartzen ditu v(16O-16O) eta v(18O-18O) isotopoen kasuetan hurrenez hurren.
- O-O lotura as a spring konsideratzen, absorbantziaren uhin-luzera, v kalkulatu ahal da.
- non k loturaren spring konstantea da, c argiaren abiadura, eta 𝝁 A-B sistemaren masa laburtuta da.
- mi i atomoaren masa da).
- 16O–16O eta 18O–18O masa laburbilduak 8 eta 9 bezala hartzen ditugu hurbilketa bat egiten. Orduan
- non ʋ uhin-zenbakia da [uhin-zenbakia= frekuentzia/argiaren abiadura].



