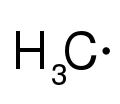Erreakzio bitarteko
Erreakzio bitartekoa da erreakzio baten tarteko urratsetan eratzen den entitate edo espeziea. Erreaktiboetatik azken produktuetara daraman erreakziobidean sortzen diren entitate ezegonkorrak dira[1].
Erreakzio kimiko gehienek etapa bat baino gehiago izaten dituzte eta urrats horietako bakoitzean sortzen diren espezieak eta hurrengo batean kontsumitzen direnak dira erreakzio-bitartekoak.
Etsenplurako eman dezagun erreakzio hipotetiko hau:
- A + 2B → C + D + E
bere erreakziobidea hauxe da:
- A + B → C + X
- X → D + Y
- B + Y → E
X eta Y erreakzio-bitartekoak dira.
Erreakzio-bitartekoek oso bizitza laburra izaten duten eta oso kasu gutxitan isolatzen dira. Normalean N2O2, NO3 edo H2I bezalako molekula ez-ohizkoak izaten dira edo I bezalako atomo askeak. Beste askotan erradikal askeak, karbokatioiak edo karbanioiak izan daitezke[2].
Adibideak[aldatu | aldatu iturburu kodea]
-
Metilo erradikala
-
Metilo kabokatioia
-
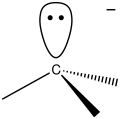
Karbanioia
Erreferentziak[aldatu | aldatu iturburu kodea]
- ↑ «ZT Hiztegi Berria» zthiztegia.elhuyar.eus (Noiz kontsultatua: 2021-01-20).
- ↑ Basterretxea, Francisco; Zabala, Gorka; Mijangos, Fernando; Izurieta, Itziar; Etxeberria, Nestor & Martinez de Marigorta, Edorta. (1999). Kimika orokorra. UEU, 273-285 or. ISBN 84-86967-71-6..