Ekuazio kimiko
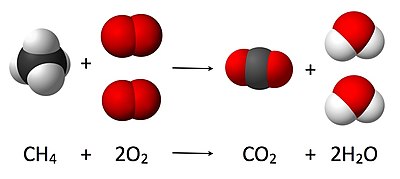

Ekuazio kimikoa erreakzio kimiko baten adierazpen idatzi eta laburtua da, erreakzio horren deskripzio kualitatibo eta aldi berean kuantitatiboa ematen duena. Erreakzioaren aurreko osagaiak erreaktiboak eta emaitzak produktuak.
Ekuazio kimikoak aurreikusten du bi produktu kimiko edo gehiago elkarlanean nola arituko diren. Substantzia kimikoen jokaerei buruz dakiguna kontuan hartuta, substantzia horien letra-sinboloak batzen ditugu matematikako problema izango balitz bezala. Horrela, aldez aurretik igarri dezakegu, substantzia kimiko bi edo gehiago nahasten ditugunean, ea produktu kimiko berria lortuko dugun eta produktu kimiko hori zein izango den.
Ekuazio kimikoak elementuen ikurren bidez adierazten ditugu, eta elementuen kantitatea eta zer egoeratan dauden ere adierazten dugu: solidoa (s), likidoa (l), gasa (g) edo akuosoa (aq).
Esate baterako: sodio kloruroaren soluzio akuosoa [NaCl (aq)] zilar nitratoaren soluzio akuosoarekin [AgNO3 (aq)] nahasten dugunean, sodio nitrato akuosoa [NaNO3 (aq)] eta zilar kloruro solidoa [AgCl (s)] osatzen ditugu.
Ikurrak erabilita, honela adierazten dugu:
NaCl (aq) + AgNO3 (aq) → NaNO3 (aq) + AgCl (s)
Bi soluzioek AgCl solidoa osatzen dute. Eraketa hori hauspeakin-erreakzioa da. Izan ere, bi soluzioak erreakzionatu eta gero, hauspeakina sortzen da, ekoizpen solidoa ez baita desegiten baina beste produktu guztiak bai.
Ekuazio kimikoen ezaugarriak[aldatu | aldatu iturburu kodea]
Ekuazio kimikoetan, sistema itxietan bezala, materia ez da sortzen eta ez da suntsitzen. Materia kontserbatzeko legeak betetzeko, ekuazio kimikoak orekatua izan behar du. Erreaktiboen aldean dauden elementuen atomo kopurua eta produktuen aldean dauden elementuen atomo kopurua bera bada, orduan, ekuazio kimikoa orekatua da.
Saio-erroreen metodoa erabilita orekatzen ditugu ekuazio kimikoak. Ekuazioa orekatzeko, erreaktiboen eta produktuen kopuruak aldatu behar ditugu bien kopurua bera izan arte. Beharrezkoa denean, molekula bakoitzaren aurrean koefizienteak jarri behar ditugu. Ekuazio bat orekatzean, azpiindizeak ez ditugu inoiz aldatu behar, hori egiteak substantzia aldatzen duelako. Elementu bakoitzaren atomo kopurua zehazteko, substantziaren koefizientea bider formula bakoitzaren azpiindizeak egin behar dugu.
Ekuazio kimikoak adieraztea eta orekatzeko metodoak[aldatu | aldatu iturburu kodea]
Ekuazio kimikoak sinboloz bidez adierazten du erreakzio kimikoa. Erreaktiboen substantzia kimikoak erreakzio kimikoaren ezkerreko aldean jartzen ditugu, produktuen substantzia kimikoak eskuinaldean, eta erdian gezia (→) jartzen dugu. Masaren kontserbazioaren legearen arabera, esan bezala, erreakzio kimikoek ezin dute atomorik sortu edo suntsitu. Gainera, elementu bakoitzari dagokionez, erreaktiboetan dauden atomoen kopuruak produktuetan dauden atomoen kopurua orekatu behar du.
Ekuazio kimikoa orekatzeko bi metodo daude:
- Lehenengoa, ikuskapen-metodoa da, eta oinarrizkoa da. Hobeto funtzionatzen du erreakzio sinpleetarako. Konplikatuagoek ahalegin handiagoa eskatzen dute.
- Bigarrena, metodo numerikoa da. Ekuazio kimikoa betetzen duten koefizienteak existitzen badira, erreakzioa orekatuta egongo da. Baina ekuazio kimikoa betetzen ez duten koefizienteak egon ezean, erreakzioa ezin da orekatu; beraz, ezinezkoa da naturan gertatzea.
