Amina
Appearance
Kimika organikoan, aminak oinarrizko nitrogeno atomo bat eta bikote bakarti bat duten konposatuak edo talde funtzionalak dira. Aminak amoniakoaren deribatuak dira, hidrogeno atomo bat edo gehiago ordezko batekin (alkilo batekin edo arilo batekin, esaterako) ordeztuta dutenak. Amina multzo garrantzitsuak daude, adibidez aminoazidoak, amina biogenikoak, trimetilamina edo anilina.
Amoniakoaren deribatu inorganikoei ere amina deritze.
Karbonilo talde bati lotutako nitrogeno atomo bat duten konposatuak, berriz, amidak dira. Horiek beste ezaugarri kimiko batzuk dituzte.
| Amina primarioa | Amina sekundarioa | Amina tertziarioa |
|---|---|---|
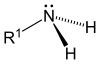
|

|
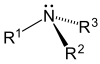
|
Kanpo estekak
[aldatu | aldatu iturburu kodea]
| Artikulu hau kimikari buruzko zirriborroa da. Wikipedia lagun dezakezu edukia osatuz. |
