Glioxal
| Glioxal | |
|---|---|
 | |
| Formula kimikoa | C2H2O2 |
| SMILES kanonikoa | 2D eredua |
| MolView | 3D eredua |
| Konposizioa | oxigeno eta karbono |
| Mota | biogenic acyclic aldehyde (en) |
| Ezaugarriak | |
| Fusio-puntua | 15 °C |
| Irakite-puntua | 50,4 °C (101,325 kPa) |
| Masa molekularra | 58,005 Da |
| Arriskuak | |
| NFPA 704 | |
| Identifikatzaileak | |
| InChlKey | LEQAOMBKQFMDFZ-UHFFFAOYSA-N |
| CAS zenbakia | 107-22-2 |
| ChemSpider | 7572 |
| PubChem | 7860 |
| Reaxys | 1732463 |
| Gmelin | 34779 |
| ChEMBL | CHEMBL1606435 |
| ZVG | 28700 |
| EC zenbakia | 203-474-9 |
| ECHA | 100.003.160 |
| CosIng | 34157 |
| MeSH | D006037 |
| RxNorm | 4967 |
| Human Metabolome Database | HMDB0303107 |
| KNApSAcK | C00059081 |
| UNII | 50NP6JJ975 |
| KEGG | C14448 |
| PDB Ligand | GXT |
Glioxala OCHCHO formulako konposatu organikoa da dialdehidoen familiakoa bi aldehido talde baititu egituran. Solido kristalinoa zuria da tenperatura baxuetan, baina horitu egiten da fusio-puntura hurbiltzean (15º C). Likidoa horia da eta lurrundurik berdea.
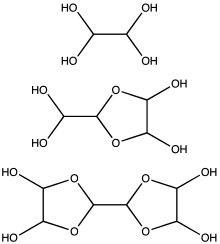
Glioxal hutsa izatea ez da ohikoa hidratatu eta oligomeroak eratzen dituelako. Hala ere, horrek ez du arazorik sortzen bere erabilera askotarako[1][2].
Glioxala aztarna-gas moduan agertzen da atmosferan hidrokarburoen oxidazioz sortua[3].
Produkzioa[aldatu | aldatu iturburu kodea]
Heinrich Debus kimikari alemanak prestatu zuen lehen aldiz glioxala etanola azido nitrikoz erreakzionaraztean[4].
Bi manera daude glioxal komertziala prestatzeko[1]:
- etilen glikola gas moduan oxidatuz zilar- edo kobre-katalizatzaile bat usatuz,
- edo azetaldehido likidoa azido nitrikoz oxidatuz,
Glioxal komertziala normalean % 40ko ur-disoluziotan saltzen da.
Erabilera[aldatu | aldatu iturburu kodea]
Glioxala kuxe papera egiteko eta ehungintzako akabera-prozesuetan baliatzen da, zimurtzen ez diren oihalak lortzeko, etsenplurako[1].
Polimeroen kimikan disolbatzaile eta saretze-agente moduan erabiltzen da.
Kimika organikoan konposatu konplexuagoak sintetizatzeko lehengai moduan baliatzen da, imidazolaren moduko heterozikloak sintetizatzeko adibidez.
Histologian finkatzaile moduan usatzen da.
Erreferentziak[aldatu | aldatu iturburu kodea]
- ↑ a b c (Ingelesez) Karpov, Andrey; Walsdorff, Christian; Siemer, Michael; Mattioda, Georges; Blanc, Alain. (2021). «Glyoxal» Ullmann's Encyclopedia of Industrial Chemistry (John Wiley & Sons, Ltd): 1–11. doi:. ISBN 978-3-527-30673-2. (Noiz kontsultatua: 2021-11-28).
- ↑ (Ingelesez) PubChem. «Glyoxal» pubchem.ncbi.nlm.nih.gov (Noiz kontsultatua: 2021-11-28).
- ↑ (Ingelesez) Vrekoussis, M.; Wittrock, F.; Richter, A.; Burrows, J. P.. (2009-07-14). «Temporal and spatial variability of glyoxal as observed from space» Atmospheric Chemistry and Physics 9 (13): 4485–4504. doi:. ISSN 1680-7316. (Noiz kontsultatua: 2021-11-28).
- ↑ (Ingelesez) Debus, H. (1857). "On glyoxal. Philosophical Magazine, 4th series, 13, 66. or..


![{\displaystyle {\ce {CH2OHCH2OH + O2 ->[Cu,Ag] CHOCHO + 2 H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1f1cb88d69a0b18323a06be73331493140d7bb1b)
![{\displaystyle {\ce {CH3OH ->[HNO3] CHOCHO}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/49946f36b81e01f1bf18bdde5b9343c6b6214595)