Orbital molekularren teoria
Orbital molekularren (OM) teoria elektroiak ondoan dauden atomoen arteko lotura bakar bati egokituta egon beharrean, molekula guztiaren nukleo atomikoen eraginpean mugitzen direla adierazten duen hurbilketa da. Hurbilketa honen arabera, atomoen izaera galdu egiten da molekularen izaeraren barruan. Hurbilketa hau lotura kimikoa determinatzeko erabiltzen da.[1] Molekulen propietate espazial eta elektronikoak mekanika kuantikoari esker daude antolatuta, eta horrela, teoria honen arabera molekuletan osatzen diren orbitalak molekula osoan zehar delokalizatuta daude, eta ez lokalizatuta bi atomoen artean balentzia lotura (BL) teorian bezala.
Orbital atomikoek atomo bati dagozkion elektroiak deskribatzen dituzten bitartean, orbital molekularrek, molekula batean dauden elektroiak deskribatuko dituzte, goian aipatu bezala, molekula guztian zehar delokalizatuta egon daitezkeelarik. Orbital molekularren teoriak, XX. mendearen hasieran proposatua izan zena, loturen ikerketa goitik behera aldatu zuen lotutako elektroien posizioak -orbital molekularrak- orbital atomikoen konbinazio lineal bezala aurkeztu zituenean (LCAO).
Planteamendua: Born Oppenheimerren hurbilketa
[aldatu | aldatu iturburu kodea]Molekulen inguruan ari garenez, beraien egoerak kalkulatzeko Schrödinger ekuaziotik abiatuko gara. Horrelako ekuazio bat dugu, denborarekiko independentea dena: . Azken honen gakoa, operadorea zein den jakitea da. Molekulen kasuan, nukleo bat baino gehiago ditugu, eta beraz, nukleoen energia zinetikoa kontutan hartu behar da. Honetaz gain elektroien energia zinetikoa, nukleo eta elektroien arteko erakarpena, nukleoen arteko errepultsioa eta elektroien arteko errepultsioa kontsideratuko dira, ondorengo operadorea lortuz:
- .
Lortu dugun ekuazio hau, ezin dugu zehaztazunez ebatzi, beraz, hurbilketa bat egin behar dugu, Born-Oppenheimerren hurbilketa deritzona. Hurbilketa honetan, nukleoen eta elektroien mugimendua desakoplatuta dagoela kontsideratzen da, eta horrela goiko ekuazioa bitan bana daitezke, alde batetik ekuazio elektronikoa eta bestetik ekuazio nuklearra lortuz.
(Ekuazio nuklearra)
(Ekuazio elektronikoa)
Modu honetan, ekuazio konplikatu bat bi ekuazio sinpleagotan banatzea lortu dugu. Ekuazio elektronikoan erabilitako operadorean, elektroien energia zinetikoa, elektroien arteko errepultsioa eta elektroi-nukleo elkarrekintza biltzen dituzten terminoak sartzen ditugu.
- .
Ekuazio elektroniko hau ere modu zehatz batean ebatzi ezin denez elektroi askoren kasuan, hurbilketaren bat egn behar da. Orbital molekularraren teoria, goiko ekuazio elektronikoa ebazteko erabili daitekeen hurbilketetako bat da.
Aplikazio kuantitatiboa
[aldatu | aldatu iturburu kodea]Teoria honetan, molekula bakoitzak orbital molekular multzo bat du, non onartzen den orbital molekularraren uhin funtzioa ψj, χi-ren eratzaile diren n orbital atomikoen konbinaketa lineal baten hurbilketa moduan idatzita dagoela, hurrengo ekuazioaren arabera:[2]
Numerikoki cij koefizienteak determinatu daitezke ekuazio hau Schrödinger ekuazio batengatik ordezkatuz eta bariazio printzipioa aplikatuz. Bariazio printzipioa mekanika kuantikoan orbital atomikoaren oinarri bakoitzaren koefizienteak eraikitzeko erabiltzen den teknika matematiko bat da. Orbital Atomikoen Konbinazio Lineak kualifikatzeko metodo hau kimika konputazionalean erabiltzen da. Eraldaketa unitario osagarri bat sisteman aplikatu daiteke konbergentzia bizkortzeko eskema konputazional batzuetan. 1930. hamarkadan, orbital molekularraren teoria balentzia loturaren lehiakide bat bezala ikusi zen, baina geroago konturatu ziren bi metodoak oso erlazionatuta daudela eta garatzen direnean baliokide bihurtzen direla. Balentzia guztietarako orbital molekularren metodo berriek elektroi-interakzioaren Lebesgue-ren integraletan oinarritzen dira, eta inbarianteak diren emaitzetarako, biraketa eta eskala- eta jatorri- aldaketak ere onartzen dituzte.
Aipatu bezala, orbital molekularrak sortuko ditugu,orbital atomikoen konbinaketa linealak bezala. Konbinaketa linealaren koefizienteak (Cn), ekuazio sekularraren bitartez determinatzen dira, hots, .
Orbital motak
[aldatu | aldatu iturburu kodea]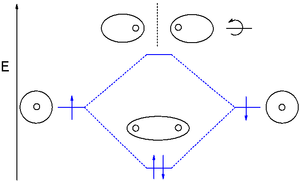
Orbital molekularren (OM) teoriak orbital atomikoen konbinazio linealak (LCAO) erabiltzen ditu orbital molekularrak eratzeko. Honetan, atomoak elkarren artean loturak eratzen dituzte. Hiru mota ezagutzen dira, orbital lotzaileak, orbital antilotzaileak eta orbital ez-lotzaileak. Orbital lotzaileetan, elektroi dentsitatea bi atomoen arteko zonaldean kontzentratzen da, beraz, dentsitate elektroniko honek bi nukleoen erakarpena eragingo du, bi atomoak batera mantenduz.[3] Orbital antilotzaileak aldiz, elektroi dentsitatea nukleo bakoitzaren atzean kontzentratzen dute, hau da, beste atomotik urrunen dagoen atomoaren aldean. Era honetan, elektroi dentsitateak nukleoa erakartzean, bi atomoen distantzia handituko du, hauen arteko lotura ahulagoa eginez. Orbital ez-lotzaileko elektroiak ez dute elkar eragiten positiboki edo negatiboki orbital atomikoetan, beraz, ez dituzte loturak ahultzen edo sendotzen.[3]
Orbital molekularrak azken hauek osatzen dituzten orbital atomikoen araberakoak dira. Sustantzi kimikoak, lotura interakzioak eratuko dituzte azken hauen orbitalen energia txikiagoa bihurtzen bada interakzioak izaterakoan. Loturak dituzten orbital desberdinak daude, konfigurazio elektronikoaren (elektroi-lainoa) eta energia mailaren araberakoak.
Molekula baten orbital molekularrak orbital molekular diagrametan adierazi daitezke.
Gainbegirada
[aldatu | aldatu iturburu kodea]Orbital Molekularraren teoriak lotura kimikoari buruzko ikuspuntu oso eta deslokalizatu bat ematen du. OM teorian, molekula batean dagoen edozein elektroi molekularen edozein lekutan aurkitu daiteke. Hau guztia gertatzen da kondizio kuantikoek nukleoen hautazko kopuru handi baten eraginpean elektroiak mugitzea baimentzen dutelako, beti ere zenbait arau kuantikok baimendutako berezko egoeratan daudela. Horrela, beharrezkoa den energiarekin kitzikatzen direnean maiztasun handiko argi edo beste baliabide batzuen bidez, elektroiak energia handiagoko orbital molekularretara igaro daitezke. Adibidez, hidrogenozko molekula diatomiko baten kasu errazean, elektroi bakar baten igoera orbital lotzaile batetik orbital antilotzaile batera, UV erradiaziopean gertatu daiteke. Igoera honek bi hidrogeno atomoen arteko lotura ahuldu egiten du eta fotolisia eman daiteke, hau da, argiaren absortzio bidezko lotura kimiko baten haustura.
Nahiz eta OM teorian orbital molekular batzuek atomo molekularren bikote espezifikoen artean lokalizatuagoak dauden elektroiak eduki ditzaketen, beste orbital batzuk molekulan zehar era uniformeago batean hedatzen diren elektroiak eduki ditzakete. Beraz, orokorrean, lotura askoz ere deslokalizatuago dago OM teorian, azken hau lotura ordena ez-oso baliokideak dituzten erresonantzia-molekulentzako teoria baliogarriagoa izanik balentzia loturaren (BL) teoria baino. Honek OM teoria sistema hedatuen deskribapenerako erabilgarriagoa izatea egiten du.
Adibideak
[aldatu | aldatu iturburu kodea]
Adibide bat bentzenoaren (C6H6) OMaren deskribapena izan daiteke, sei karbono atomo eta hiru lotura hirukoitzez osatutako eraztun hexagonal aromatikoa izanik. Molekula honetan, balentzia loturako 30 elektroi totaletatik 24, hau da, karbono atomoetatik eratorriak diren 24 eta hidrogeno atomoetatik eratorriak diren 6, 12σ (sigma) orbital lotzailetan kokatuak daude, bereziki atomo bikote (C-C edo C-H) artean jarrita daudenak, balentzia loturako deskribapenean dauden elektroien antzera. Bestetik, bentzenoan, gainerako sei lotura elektroiak eraztunaren inguruan deslokalizatuak dauden hiru π (pi) orbital molekular lotzaileetan kokatuak daude. Elektroi hauetako bi, sei atomo horiek bezalako kontribuzio orbitalak dituen OM batean daude. Beste lau elektroiak, angelu zuzenen arteko nodo bertikalak dituzten orbitaletan daude. Balentzia loturaren teorian bezala, sei π elektroi deslokalizatu hauek guztiak eraztunaren plano gainetik eta azpitik dagoen tarte handiago batean daude. Bentzenoaren karbono-karbono lotura guztiak kimikoki baliokideak dira. OM teorian, hau hiru π orbitalak konbinatzearen eta sei karbono atomoen gain sei elektroi gehigarriak uniformeki banatu izanaren ondorio bat da.

Metanoa (CH4) bezalako molekuletan, bere 8 balentzia elektroiak 4 orbital molekularretan daude banatuta, hauek 5 atomoetan zehar banatuta daudelarik. Hala ere, esan beharra dago, orbital molekular horiek 4 sp3 orbital lokalizatu bilakatu daitezke. Linus Paulingek 1931an, karbonoaren 2s eta 2p orbitalak hibridatu zituen, modu honetan, zuzenean hidrogenoaren 1s orbitalari oinarrizko funtzioak ezartzen ziren, gainezartze maximoa kontuan hartuz. Bestalde, orbital molekular deslokalizatuen deskribapena ionizazio energia eta espektroen absortzio banden posizioa aurresateko metodo egokiagoa da. Metanoa ionizatzen denean, elektroi bakarra hartzen da balentzia orbital molekularretatik, s loturatik edo degeneratutako p lotzaile mailetatik etor daitekeena, bi ionizazio energia sortuz. Hauen konparaketa eginez gero, VB teoria zailagoa da azaltzeko, izan ere elektroi bat sp3 orbitaletik mugitzen denean erresonantzia lau balentzia loturen artean gertatzen da, non bakoitzak elektroi bakarreko lotura sinple bat eta bi elektroiko hiru lotura dituen. Hiru aldiz degeneratutako T2 eta A1 estatu ionizatuak (CH4+) sortzen dira lau egitura hauen konbinazio lineal ezberdinak eginez. Ionizatutako estatuaren eta oinarri estatuaren arteko energia diferentziak bi ionizazio energiak emango dizkigu.
Bentzenoan bezala, substantzia batzuetan (hala nola klorofila, beta karoteno eta hemo taldeak) π orbitaletako elektroi batzuk orbital molekularren artean zabaltzen dira distantzia handietan zehar molekularen barruan, energia baxuagotan (espektro ikuskorrean) absortzioa ematen delarik eta honek substantzia hauek kolore bereizgarriak azaltzen ditu.[4] Hau eta molekulen beste datu espektroskopiko batzuk oso ondo azalduta daude orbital molekularraren teoriaren bidez. Bestalde, orbital molekularraren teoriak molekulen konduktibitate elektrikoa ere azaltzen du, izan ere, p orbital erdi beteak akoplatzean, banden artean dagoen elektroi mugimenduak, konduktibitate elektrikoa izatea eragiten du.
Erreferentziak
[aldatu | aldatu iturburu kodea]- ↑ Daintith, J. (2004). Oxford Dictionary of Chemistry. New York: Oxford University Press. ISBN 0-19-860918-3.
- ↑ Licker, Mark, J. (2004). McGraw-Hill Concise Encyclopedia of Chemistry. New York: McGraw-Hill. ISBN 0-07-143953-6.
- ↑ a b Miessler and Tarr (2013), Inorganic Chemistry, 5th ed, 117-165, 475-534.
- ↑ Griffith, J.S. and L.E. Orgel. "Ligand Field Theory". Q. Rev. Chem. Soc. 1957, 11, 381-383
Kanpo estekak
[aldatu | aldatu iturburu kodea]- Molecular Orbital Theory - Purdue University
- Molecular Orbital Theory - Sparknotes
- Molecular Orbital Theory - Mark Bishop's Chemistry Site
- Introduction to MO Theory - Queen Mary, London University
- Molecular Orbital Theory - a related terms table
- An introduction to Molecular Group Theory - Oxford University







