Silizio dioxido
| Silizio dioxido | |
|---|---|
 | |
| Formula kimikoa | SiO2 |
| SMILES kanonikoa | [Si=O&zoom=2.0&annotate=none 2D eredua] |
| MolView | [Si=O 3D eredua] |
| Konposizioa | oxigeno eta silizio |
| Mota | covalent network solid (en) |
| Ezaugarriak | |
| Disolbagarritasuna | 0,12 g/L (ur, ezezaguna) 0,9 g/L (ur destilatu, 200 °C) |
| Fusio-puntua | 1.710 °C |
| Irakite-puntua | 2.230 °C (760 Torr) |
| Lurrun-presioa | 0 mmHg (20 °C) |
| Masa molekularra | 59,967 Da, 60,0843 g/mol eta 60,038 g/mol |
| Arriskuak | |
| NFPA 704 | |
| Identifikatzaileak | |
| InChlKey | VYPSYNLAJGMNEJ-UHFFFAOYSA-N |
| CAS zenbakia | 7631-86-9 |
| ChemSpider | 22683 |
| PubChem | 24261 |
| Reaxys | 3902804 |
| Gmelin | 30563 |
| ChEBI | 200274 |
| ChEMBL | CHEMBL3188292 |
| RTECS zenbakia | VV7565000 |
| ZVG | 1290 |
| DSSTox zenbakia | VV7565000 |
| EC zenbakia | 231-545-4 |
| ECHA | 100.028.678 |
| CosIng | 78845 eta 38146 |
| MeSH | D012822 |
| RxNorm | 9771 |
| Human Metabolome Database | HMDB0035659 |
| UNII | ETJ7Z6XBU4 |
| NDF-RT | N0000145795 |
| KEGG | C19572 |
Silizio dioxidoa edo silizea (SiO2) silizio eta oxigenoz osatutako konposatu bat da. Kuartzoaren eta silikato guztien oinarrizko konposatua da eta beraz mineral gehienena. Harearen konposatu nagusia izanda porlana, beira eta keramika egiteko erabiltzen da.
Barne egitura
[aldatu | aldatu iturburu kodea]Kuartzoa silikato bat da, eta tektosilikato taldearen barruan kokatzen da. Kuartzoak 9 polimorfo ditu[1]: kuartzo baxua (α), kuartzo altua (β), tridimita baxua (α), tridimita altua (β), kristobalita baxua (α), kristobalita altua (β), koesita baxua (α), koesita altua (β) eta esitshovita.
Polimorfo hauek guztiak elektrikoki neutroak dira eta hiru kategoria estrukturaletan sailkatzen dira:
- α QTZ-a (kuartzo baxua): Simetria gutxiko egitura du. Sare trinkoa dauka.
- α Tridimita: α QTZ-ak baino simetria gehiago dauka eta sare irekiagoa.
- α Kristobalita: Simetria handiena duen kategoria; sarea ere irekiena duena da.
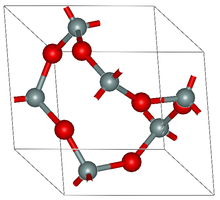
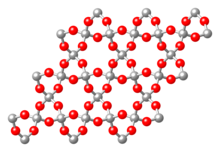
α-tik β-ra pasatzeko, mineralek energia xurgatu behar dute, eta alderantziz; β-tik α-ra pasatzeko energia kopuru konstantean askatu behar dute. Ondorioz, α-tik β-rako aldaketa tenperatura igoera batekin batera ematen da eta β-tik α-rakoa, berriz, tenperatura jeitsiera batekin batera. Aipagarria da tenperatura baxuko formek simetria gutxiago dutela altukoek baino: adb, α tridimitak simetria gutxiago dauka β tridimitak baino.
Mineralaren izena mantentzen denean (adb., kuartzo baxua izatetik kuartzo altua izatera pasatzen denean), desplazamendu polimorfismoa egon dela esaten da. Hau da, atomoen arteko loturak apurtu beharrean, tetraedroak lekuz aldatu dira energia gutxi erabiliz. Alderantzizkoa gertatzen da mineralen izena aldatu dadin (adb., kuartzo altua izatetik tridimita baxua izatera pasatzen delarik). Kasu honetan, loturak apurtu egin dira berriak sortuz, eta honetarako energia handia behar izaten da.
Azpimarratu daiteke koesita eta estishovita dentsitate altuko polimorfoak direla, baita tenperatura handian daudenean ere.
Non eta zer mineralekin aurkitu dezakegun
[aldatu | aldatu iturburu kodea]Kuartzoa hiru arroka motetan aurkitzen da: arroka metamorfikoetan (gneissetan, eskistoetan), arroka sedimentarioetan (hareharrietan, konglomeratuetan) eta arroka igneoetan (pegmatita, granito zein granodioritatan).
Feldespato potasikoarekin, plagioklasekin, biotitarekin, moskovitarekin, kloritarekin, granatearekin, epidotarekin, anfibolarekin, lepidolitarekin, piritarekin edota kaltzitarekin batera ager daiteke, besteak beste.
Identifikazioa
[aldatu | aldatu iturburu kodea]Hauek dira kuartzoa identifikatzeko erabiltzen diren irizpideak:
- Gogortasuna 7-koa du, eta beraz, beira marratzen du.
- Zuria edo kolorgea da gehienetan (arrosa ere izan liteke).
- Ez du exfoliaziorik, masa irregular baten gisan aurkezten zaigu.
- HCL azido klorhidrikoa bota ezkero, ez dugu erreakziorik ikusiko. Kaltzitarekin bai, ordea.
Mikroskopiotik begiratu ezkero[2][3]:
- PPL-n:
- Kolorgea
- Xenomorfoa
- Exfoliazio gabea
- Alteraziorik gabea
- Erliebe baxukoa
- XPL-n[4]:
- Itzaltze zuzenduna
- Uhin-itzaltzea
- 1go ordeneko zuri, gris, horixka interferentzia koloreak.
Erreferentziak
[aldatu | aldatu iturburu kodea]- ↑ (Gaztelaniaz) Cornelis Klein/Cornelius S. Hulrbut,Jr; Manual de Mineralogia basada en la obra de J.D. Dana, vol.2, 13. kapit., 13.6 atala. Editorial Reverté, ISBN 978-84-291-4607-3
- ↑ (Ingelesez) Introduction to Optical Mineralogy, William D. Nesse. ISBN:978-0-19-539115-2
- ↑ (Gaztelaniaz) Minerales en lámina delgada, 15-16.or. Dexter Perkins eta Kevin R. Henke, ISBN 84-205-3552-4
- ↑ (Ingelesez) Mineralogy and optical mineralogy; Dyar, Melinda Darby & Gunter, Mickey E.
Kanpo estekak
[aldatu | aldatu iturburu kodea]- (Ingelesez) Kuartzoari buruzko webgunea

