Amino talde


Amino taldeak amoniakoaren deribatuak dira. Aminak amoniakoaren deribatuak dira, non protoi bat edo gehiago alkilo edo arilo taldeengatik ordezkatzen diren. Aminak primario, sekundario edo tertziario bezala sailkatzen dira, hidrogenoa ez den beste ordezkapen talde kopuruaren arabera.[1][2]
Amoniako hidrogeno atomo bat R- alkilo talde batengatik ordezkatzen bada, bere formula orokorra R-NH2 da eta amina primario bati dagokio. Bi edo hiru hidrogenoz ordezkatua badago, amina sekundarioa edo tertziarioa izango da. Hauen aurkikuntza 1849.urtean izan zen eta Wurtz kimikari alemanari esleitzen zaio.
Aminak oso maiz agertzen dira naturan. Landaretatik isolatzen diren amina naturalei, alkaloide deritze. Honakoak dira alkaloideen adibideak.
Aminen Propietateak[aldatu | aldatu iturburu kodea]
Geometria[aldatu | aldatu iturburu kodea]
Amina baten nitrogeno-atomoak, orokorrean, sp3 hibridazioa izaten du elektroi bikote bakartiak sp3 orbital hibridoa okupatzen duelarik.
Irudian ikus daitekeenez, tetraedro baten itxura hartzen dute, 108° inguruko angelua dutelarik.
Azidotasuna[aldatu | aldatu iturburu kodea]
N-H lotura polarizatuta badago, lotura hau hautsi daiteke protoi bat askatzeko. Horregatik, amina primarioak eta sekundarioak ahulki azidoak dira. Lortutako anioiei amiduro deritze eta base oso sendoak (pka 35 inguru) eta nukleozale onak dira.
Basikotasuna[aldatu | aldatu iturburu kodea]
Basikotasuna aminen propietate garrantzitsua da. Orokorrean, aminak alkoholak edo eterrak baino base sendoagoak dira, eta erraz izan daitezke protonatuak, baita azido ahulekin ere.
Aminak protonatzeko duten erraztasun hori erabilgarria da beste substantziekin osatutako nahaste organikoetatik banatzeko. Prozesu horri disolbatzailearen bidezko erauzketa esaten zaio. Substantzia organikoen nahaste bat disolbatzen da lehendabizi disolbatzaile organiko batean. Ondoren, disoluzio azido akuoso bat gehitzen zaio nahasteari eta indarrarekin astintzen da. Nahastea geruza organikoa eta akuosoa banatzen uzten da. Baldintza hauetan aminaren molekula gehienak protonatuak daude eta amonio ioiak osatzen dituzte. Amonio ioiak karga dute; ondorioz, fase akuosoan disolbagarriagoak dira fase organikoan baino. Fase akuosoaren banaketak amonio ioien erauzketa bideratzen du. Gero, base batekin tratatuko dira amina neutroa berreskuratzeko.
Prozesu hori asko erabili zen XIX. mendean aminak landare-estraktuetatik banatzeko. Aspalditik jakin da posible dela landareetatik aminak isolatzea beraien propietate basikoak aprobetxatuz. Hori dela, eta landareetatik ateratako aminei alkaloideak (alcalino hitzetik eratorria, zeinak basiko esan nahi duen) deritze.
Ondorioa: aminak, ura bezala, anfoteroak dira protoi bat eman edo har dezaketelako.
Polartasuna[aldatu | aldatu iturburu kodea]
Aminak polarrak dira, baina alkoholak polarragoak.
Aminaren polartasuna momentu dipolarrean oinarritzen da. Elektroi-bikote bakartiaren momentu dipolarra C-N eta H-N loturek sortutako momentu dipolarrari gehitzen zaio oso momentu dipolar handia sortuzen duelarik.
Fusio- eta Irakite-Puntua[aldatu | aldatu iturburu kodea]
Alkanoek baino irakite-puntu altuagoak dituzte; hala ere, alkoholek irakite-puntu altuagoak dituzte[3].
Amina primario eta sekundarioek hidrogeno-loturak eratzen dituztenez, alkanoek baino irakite-puntu altuagoak dituzte, baina alkoholenak baino pixka bat baxuagoak, aminek sortzen dituzten hidrogeno-loturak ahulagoak baitira. Amina tertziarioek, berriz ezin dute hidrogeno-loturarik sortu, nitrogenoan hidrogenorik ez dagoelako. Horregatik, amina tertziarioen irakite-puntuak pisu molekular antzeko amina primario edo sekundarioenak baino baxuagoak dira.
N-H loturak ahulagoak dira O-H loturak baino; ondorioz, nahiz eta alkoholek eta aminek masa molekular antzekoak izan, aminen irakite-puntuak alkoholenak baino baxuagoak dira.
Disolbagarritasuna[aldatu | aldatu iturburu kodea]
Disolbagarritasun altua dute.
Amina primarioak eta sekundarioak, polarrak direnez, hidrogeno-zubiak osatzen dituzte elkarrekin, baita urarekin ere; ondorioz, uretan disolbatzen dira.
6 karbono baino gehiagoko aminek zailtasunak dituzte uretan disolbatzeko. Azido diluituetan, aminek amonio-gatzak sortzen dituzte, eta uretan erraz disolbatzen dira.[3]
Aminen Erreaktibitatea[aldatu | aldatu iturburu kodea]
Amina batek duen nitrogenoak elektroi bikote bakartia du. Nitrogenoak, dentsitate elektroniko altuko gunea adierazten du. (ikus irudia). Elektroi bikote bakarti hori aminen erreakzioen erantzulea da. Izan ere, bikote bakartiak base nahiz nukleozale bezala joka dezake.
-
Base bezala
-
Nukleozale bezala
Aminen Erabilera[aldatu | aldatu iturburu kodea]
Aminak oso erabiliak dira industrian: kosmetikan, farmakologian, oihalgintzan, ile tindatzaileen industrian, koloratzailetan eta kautxuaren antioxidatzaile bezala. Adibidez: adrenalina, morfina, nikotina, etab.
Izendaketa edo Nomenklatura[4][aldatu | aldatu iturburu kodea]
Aminak konposatu organikoak dira eta amoniakoaren deribatuak kontsidera ditzakegu. Aminaren protoiak beste ordezkatzaile edo erradikalengatik ordezka daitezke. Aminaren protoi ordezkatuen kopuruaren arabera, amina primario, sekundario edo tertziarioak izango ditugu[4].
Irudi honetan, amina mota ezberdinak ikus ditzakegu. Lehenengo irudian amoniakoa agertzen zaigu, 3 protoiak ordezkatu gabe dituelarik. Bigarren irudian, aminaren protoi bat ordezkatzen da erradikal batez, amina primarioa sortuz. Ondorengo irudian, aminaren bi protoi ordezkatzen dira, amina sekundarioa sortuz. Azkeneko irudian, aminaren protoi guztiak ordezkaturik daude, amina tertziarioa sortuz.
Adibide bezala, etilamina, dimetilamina eta trimetilamina ditugu.
Amina primarioen nomenklatura[aldatu | aldatu iturburu kodea]
Amina primarioak, -NH2 talde funtzionala alkilo talde bati lotuta duten molekulak dira. Amina primarioak izendatzeko IUPAC arauak jarraitu behar ditugu. Aminak izendatzeko, alkilo taldearen egitura ikusi behar dugu. Izendatzen ari garen molekula alkilo talde sinple bat baldin badu, alkilaminen aurrean gaude. Hauek izendatzeko, alkilo taldea identifikatzen da, eta ondoren, -amina atzizkia eransten zaio.

Adibidez, etilaminaren kasuan, alkilo taldea etiloa da.
Alkilo taldea konplexuagoa bada, hau da, beste alkilo erradikal batzuk baldin baditu, molekula hauei alkanoamina deritze. Hauek izendatzeko, lehenengo kate nagusia aukeratu eta zenbatu behar dugu. Kate nagusia amino taldea duen katea izango da (baldin eta beste talde funtzionalik ez badago molekulan). Katea zenbatzeko, amino taldetik gertuen dagoen karbono mutur batetik hasiko gara, karbono horri 1 zenbakia jarriko diogularik. Molekulak ordezkatzaile bat baino gehiago baldin baditu, zenbakien konbinaketa ahalik eta baxuena izan behar da. Behin kate nagusia zehaztuta eta zenbatuta dugula, molekula izendatzen hasten gara. Horretarako, ordezkatzaileen lehentasuna aztertu behar dugu. Aminek beti alkiloek baino lehentasun handiagoa dute, beraz, amina talde nagusi bezala izendatuko dugu, eta erradikalak talde sekundario bezala. Amina eta erradikalen posizioa zehazten da, eta erradikalei -il atzizkia jartzen zaie. Bukatzeko, molekularen izenari -amina atzizkia jartzen zaio.
Adibidez, 3-metil-1-butanamina molekulan, kate nagusia amina taldea barruan duena da, hau da, butanoa ( 4 karbonokoa ). Amina taldea karbono mutur batean dago, beraz, karbono horri 1 zenbakia jartzen zaio. Karbono horretatik abiatuz, kate osoa zenbakitzen da. Kate nagusiaren 3. karbonoan, metilo erradikal bat dugu, beraz, erradikal hori 3-metil bezala izendatuko dugu. Amaitzeko, lehen aipatutako arauak jarraituz, molekula osoa izendatzen dugu.
Amina sekundario eta tertzioarioen nomenklatura[aldatu | aldatu iturburu kodea]
Amina primarioekin bezala, alkilamina edo alkanoamina bezala izendatu daitezke, beti ere alkil taldearen konplexutasunaren arabera. Izendatzeko, IUPAC arauak jarraituko ditugu.
Alkilo taldeak sinpleak baldin badira, orden alfabetikoan izendatzen dira, eta behin baino gehiagotan errepikatuta baldin badago, di-, tri- aurrizkiak erabiltzen dira izendatzeko.
Molekula hauek izendatzeko beste modu bat, N lokalizatzailea erabiltzea izango da. Lokalizatzaile hau erradilaka izendatu baino lehen jartzen da, honela, nitrogenoari zuzenean lotuta dauden erradikalak erraz identifikatu daitezke.
Konposatu organikoen izendapenari buruzko informazio gehiago lortzeko: konposatu organikoen nomenklatura erlaitzera joan.
Aminen lehentasuna beste talde funtzionalekiko[aldatu | aldatu iturburu kodea]
Aminen lehentasuna beste talde funtzionalekiko tabulatuta dago. Molekula batean, azido, ester, amida, aldehido, zetona edota alkohol bat izanez gero, amina talde funtzional sekundario bezala izendatuko da, eta -amino aurrizkia erabiltzen da. Molekulan aminak baino lehentasun txikiagoko molekulak bandin badaude, hala nola, eterrak, halogenoak,... amina beti talde nagusi bezala izendatuko da eta -amina atzizkia erabiliko da.
Enaminak[aldatu | aldatu iturburu kodea]
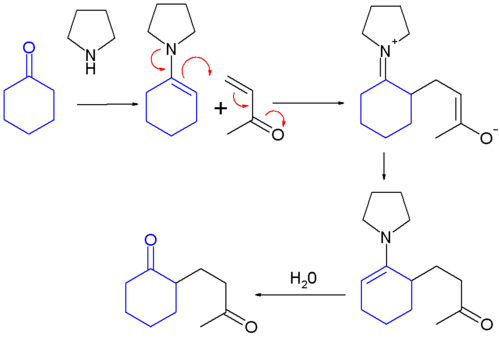
Enaminak aldehido edo zetona batek amina sekundario batekin erreakzionatzean lortzen dira[5].
Enaminaren formazio mekanismoa[aldatu | aldatu iturburu kodea]
Amina sekundarioak karboniloari egindako hasierako erasoaren ondoren, ura eliminatzen da alfa karbonilo abiapuntuan eta karboniloaren karbonoaren artean lotura bikoitza sortuz.
-
1. pausoa: karboniloaren protonazioa.
-
2.pausoa: amina sekundarioaren eraso nukleozalea.
-
3.pausoa: azido-base oreka
-
4.pausoa: uraren galera
-
5.pausoa: eliminazioa
Enaminen sintesia[aldatu | aldatu iturburu kodea]
Iminak[aldatu | aldatu iturburu kodea]
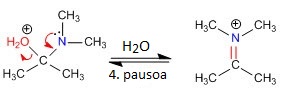
Iminak aldehido edo zetona batek amina primario batekin erreakzionatzean lortzen dira.
Iminen formazio mekanismoa[aldatu | aldatu iturburu kodea]
Iminak sortzeko karboniloak amina primario batekin erreakzionatu behar du, ur molekula bat askatuz. Ur molekula askatzea beharrezkoa da oreka desplazatu ahal izateko. Prozesu hau itzulgarria izango da.[6]
-
1.pausoa: karboniloaren protonazioa
-
2. pausoa: azido-base oreka
-
3. pausoa: ur molekularen eliminazioa
-
4. pausoa: imonio katioiaren desprotonazioa
Erreakzioak[aldatu | aldatu iturburu kodea]
Aminen prestaketa[4][aldatu | aldatu iturburu kodea]
Alkilko haluroetatik abiatuz[aldatu | aldatu iturburu kodea]
Azido karboxilikoetatik abiatuz[aldatu | aldatu iturburu kodea]
Bentzenotik abiatuz[aldatu | aldatu iturburu kodea]
Azidaren sintesia[aldatu | aldatu iturburu kodea]
Gabrielen sintesia[aldatu | aldatu iturburu kodea]
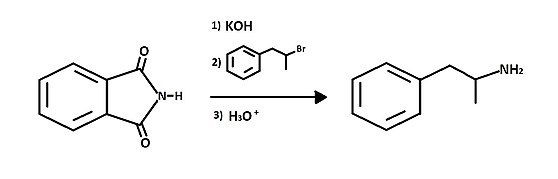
Aminen prestakuntzarako erredukzioaz baliatzen ez den bide eraginkorra Gabriel izeneko sintesia da. Prozedura honetan, azido 1,2-bentzenodi-karboxilikoaren imida base batekin desprotonatu eta gero, haloalkano egokiarekin alkilatzen da. Horrela lortutako deribatua, hidrazina edo azidoaren laguntzaz amina primario bihurtzen da.[7]
Amidazio erreduktorea erabiliz[aldatu | aldatu iturburu kodea]
Aminazio erreduktiboaz aminak lortzen dira ere. Metodo honetan, lehenengoz aldehido edo zetona batekin kondentsazioa, eta gero lortutako iminaren erredukzioa burutzen dira.[8]
Azilazioa[aldatu | aldatu iturburu kodea]
Aminen espektroskopia[4][aldatu | aldatu iturburu kodea]
Amina talde funtzional baten presentzia molekula batean identifikatzeko, normalean teknika batzuen konbinaketaren bidez egiten da, hala nola, infragorri-espektroskopia (IR), masa-espektroskopia edo erresonantzia magnetiko nuklearraren espektroskopia (RMN).
Infragorri-espektroskopia (IR)[4][aldatu | aldatu iturburu kodea]
Infragorri-espektro batean amina primario eta sekunarioen seinalea 3.350 eta 3.500 cm-1 tartean ematen dute. Seinale horiek N-H loturaren elongazioaren ondorioz agertzen dira, eta intentsitate ertaina dute.
Amina primarioek bi piko ematen dituzte seinalean, intentsitate berdinekoak; izan rere, bi hidrogenoen elongazioa nitrogenoarekiko simetrikoa da. Amina sekundarioek, aldiz, piko bakarra ematen dute. Amina tertziarioek H-H lotura ez dutenez, ez dute tarte horretan seinalerik ematen , baina azido klorhidrikoarekin tratatuz gero, 2.200 eta 3.000 cm-1 tartean ematen dute seinalea.
EMN-espektroskopia (EMN)[4][aldatu | aldatu iturburu kodea]
Aminen EMN-espektro batean edo nitrogenoari zuzenean lotuta dagoen hidrogeno atomo ( amina primario edo sekundarioetan), normalean seinale zabala 0,5 eta 5 ppm artean agertzen da. Seinalearen posizio zehatza zenbait faktoreen mende dago, hala nola disolbatzailea, tenperatura edo kontzentrazioa. Seinalearen zabalkuntza kendu daiteke, baldin eta amina ur astunean (D2O) disolbatzen bada; izan ere, aminaren protoiak deutroiekin ordezkatzen dira.
Ikus dezakegu nola nitrogenoaren eraginez, alboan dituen hidrogenoen seinalea desplazatzen dela. Nitrogeno atomoaren babesgabetasun-efektua txikitzen doa protoiak nitrogeno atomotik urrutzen direnean. Hau da, nitrogeno atomotik gertu dauden protoien seinalea ezkerrera desplazaturik egonen da.
Amina baten karbonoaren EMN ( C-EMN) espektro batean, karbonoaren atomoak, normalean, 30-50 ppm tartean agertzen dira. Hidrogenoarekin gertzten den bezala, karbono-atomoen seinalea ere desplazaturik ikusten da. Desplazamendu hori txikiagotzen doa bitrogeno eta karbono atomoen arteko distantzia handitzen denean.
Masa-espektroskopia[4][aldatu | aldatu iturburu kodea]
Amina baten masa-espektroskopia oso berezia da, izan ere, ioiak pisu molekular bakoiti batean ematen du seinalea. Ioiak pisu molekular bakoitian seinalea emateak nitrogenoaren arauak jarraitzen dituela esan nahi du. Gainera, ioiek zatikatze-patroi berezi bat dute: α apurtzea jasaten dute, ondorioz, erradikal bat eta katioi bat sortzen dira, eta katioia erresonantziaz egonkortzen da.
Aminoazidoak[aldatu | aldatu iturburu kodea]
Aminoazidoak, proteinen monomeroak dira. Hauek amino talde bat eta karboxilo talde bat dute. Bi talde funtzionalen presentziak egiten du posible bi aminoazido elkartzea.
Egitura eta propietateak[9][10][aldatu | aldatu iturburu kodea]
Aminoazidoek beren egituran gutxienez amino (-NH2), talde bat aurkezten dute, izaera basikoa duena, karboxilo (-COOH) talde bat, izaera azidokoa, kate aldakor (-R) bat eta hidrogeno bat (-H). Hurrengo irudian ikusi daitekeen bezala.

Aminoazidoak molekula anfoteroak dira, hau da, azido edo base bezala jokatu dezake aurkitzen den inguruaren pHaren arabera.
Karboxilo taldea dutenez, protoiak (-H+) askatu ditzakete, azido bezala jokatuz. Amino taldea dutenez, protoiak (-H+) onartu ditzakete, base bezala jokatuz. Ondorioz, karboxilo taldea -COO- modura geratuko litzateke eta amino taldea -NH3+ modura.
Ingurunea azidoa bada, aminoazidoak base modura jokatuko du, -COO- taldeak protoi bat hartuko du eta karga negatiboa galduko da.
Ingurunea basikoa bada, aminoazidoak base bezala jokatuko du, -NH3+ taldeak protoi bat askatuko du eta ondorioz karga positiboa galduko da.
Estereoisomeriari begiratuz, aminoazido guztiek ( glizina izan ezik) karbono asimetriko bat dute, α izenekoa, ondorioz, bi estereoisomero bereizi ditzakegu: D isomeroa eta L isomeroa.

D isomeroa: aminoazidoa Meso forman marraztean eta karboxilo taldea goran jartzean , amino taldea eskuineko aldean geratzen bada.
L isomeroa: aminoazidoa Meso forman marraztean eta karboxilo taldea goran jartzean , amino taldea ezkerreko aldean geratzen bada.
Bi isomero hauek ispiluko irudiak dira eta ezin dira gainezarri, ondorioz, enantiomeroak direla esan daiteke.
Aminoazido proteiko guztiek L konfigurazioa aurkezten dute.
Isomeria optikoari erreparatuz, esan daiteke aminoazidoek aktibitate optikoa dutela karbono asimetrikoa dutelako. Aktibitate optikoa dutenez argi polarizatua desbideratu dezakete bi norabideetan.
Dextrogiro edo (+): aminoazidoak argi polarizatua eskuinera desbideratzen duenean.
Lebogiro edo (-): aminoazidoak argi polarizatua ezkerrera desbideratzen duenean.
Esan beharra dago ez daukala zerikusirik aminoazidoaren D edo L konfigurazioak eta zein norabideetan desbideratuko duen argi polarizatua. Hau da, D konfigurazioa duen aminoazido bat dextrogiro edo lebogiro izan daiteke eta alderantziz.
Peptidoak[aldatu | aldatu iturburu kodea]
Bi aminoazido edo gehiago amida lotura bidez elkartzean sortutako molekulak dira. Proteina eta peptidoetan, amida loturari lotura peptidiko deitzen zaio. Peptidoek orokorrean 50 eta 100 aminoazido izaten dituzte eta beraien masa molekularra 500 unitate baino txikiagoa izan behar du. Masa molekularra 500 unitate baino handiagoa bada proteina kontsideratzen dira.
Lotura peptidikoa[aldatu | aldatu iturburu kodea]
Lotura peptidikoa osatzeko aminoazido baten karboxilo taldeak beste aminoazido baten amina taldearekin erreakzionatu behar du ur molekula bat askatuz.

Proteinak[aldatu | aldatu iturburu kodea]
Proteinak pisu molekular altuko biomolekulak dira. Hauek aminoazido kate linealez osatuak daude eta lotura peptidikoaren bidez lotzen dira. 100 aminoazido baino gehiago elkartzean sortzen dira orokorrean.
Amidak[aldatu | aldatu iturburu kodea]
Amidak, amina bat eta azido karboxiliko bat lotzean sortutako konposatu organikoak dira. Azido karboxilikoaren deribatuak direla ere kontsideratu daiteke non azido karboxiliko taldea amino talde batengatik ordezkatu den.
Nomenklatura[aldatu | aldatu iturburu kodea]
- Eratorritako azidoa bezala izendatzen dira “amida” atzizkiarekin[11].
- Amida ordezkatua bada, N aurrizkia aurrezarri behar da nitrogenoari lotutako erradikala zein den zehazteko.
- Karboxamida atzizkia erabiltzen da -CO-NH2 taldearentzat, erreferentziazko azidoa -karboxiliko atzizkia erabiliz izendatzen bada.
- Amida talde funtzionala ez denean lehentasuna duena, -CO-NH2 taldea Karbomoil- aurrizkiarekin idazten da eta -CO-NH-CH3 metilkarbomoil- aurrizkiarekin. -NH-CO-CH3 -azetamida bezala izendatzen da eta -NH-CO-CH2-CH2-CH3 propanokarboxamido- bezala.
Formula ematen denean[aldatu | aldatu iturburu kodea]
Hasi nitrogenoari lotutako erradikalak izendatzen N aurrezarriz. Ondoren karboniloa duen katea izendatu -amida bukaeran duela.
Izena ematen denean[aldatu | aldatu iturburu kodea]
-amida atzizkiaren aurreko erroa kate nagusia izango da. Nitrogenoaren ondoan dauden erradikalak N ren jarraian idatzi. Azkenik hidrogenoak osatu.
Erreferentziak[aldatu | aldatu iturburu kodea]
- ↑ [https://www.faidherbe.org/site/cours/dupuis/amind.htm «Les amines - Cours de chimie organique - G�rard Dupuis»] www.faidherbe.org (Noiz kontsultatua: 2018-12-13).
- ↑ www.remede.org (Noiz kontsultatua: 2018-12-13).
- ↑ a b Luis Mera Cabezas. (2013-08-29). Grupos amino. (Noiz kontsultatua: 2018-12-13).
- ↑ a b c d e f g (Gaztelaniaz) Klein, David. (2013). Química Orgánica. Editorial Medica Paramericana, 1128-1129 or. ISBN ISBN:978-84-9835-169-9..
- ↑ «Formación de Enaminas | Química Orgánica» www.quimicaorganica.net (Noiz kontsultatua: 2018-12-13).
- ↑ «Iminas | Química Orgánica» www.quimicaorganica.net (Noiz kontsultatua: 2018-12-13).
- ↑ Kimika Orokorra. Udako Euskal Unibertsitatea ISBN 84-86967-71-6..
- ↑ Kimika orokorra. Udako Euskal Unibertsitatea 1996 ISBN 8486967716. PMC 431201681. (Noiz kontsultatua: 2018-12-13).
- ↑ animaamino.gif (Imagen GIF, 400 × 400 píxeles) - Escalado (0 %). (Noiz kontsultatua: 2018-12-13).
- ↑ «Propiedades de los aminoácidos. | La guía de Biología» biologia.laguia2000.com (Noiz kontsultatua: 2018-12-13).
- ↑ «Amidas» www.alonsoformula.com (Noiz kontsultatua: 2018-12-13).